TE RECOMENDAMOS
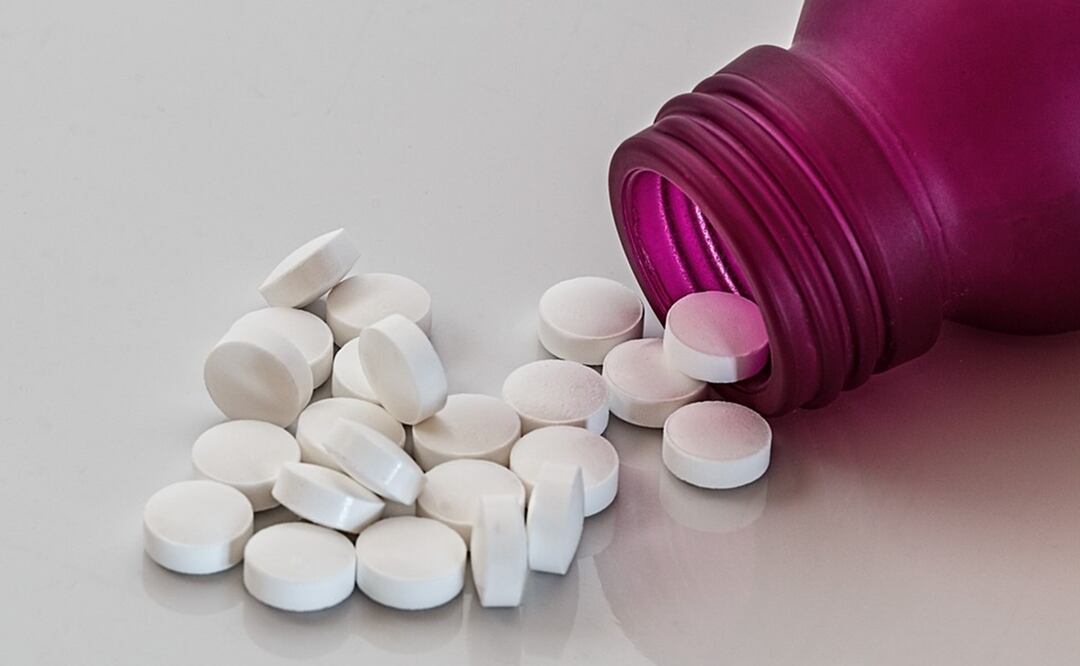
Lupin Pharmaceuticals Inc., una marca de medicamentos para la presión arterial alta está retirando una línea de tabletas por altos niveles de impurezas que causan cáncer.
De acuerdo con una alerta emitida por la Administración de Medicamentos y Alimentos de Estados Unidos (FDA por sus siglas en inglés), la línea de tabletas de Irbesartan e Hidroclorotiazida para tratar la presión arterial ha sido retirada voluntariamente luego de que se encontra compuestos de N-nitrosoirbesartan en su fórmula.
Esta impureza es un posible carcinógeno humano, según las investigaciones, y fue encontrado en altos niveles en las tabletas, muy por encima del límite de su uso.
“Como parte de la evaluación en curso de Lupin, el análisis reveló que ciertos lotes de API probados (pero no los lotes de productos terminados) estaban por encima del límite de especificación para la impureza, N-nitrosoirbesartan”, señala la FDA en su informe.
La marca comenzó con el retiro de algunos lotes, incluidos Irbesartan Tablets USP de 75 mg, 150 mg y 300 mg e Irbesartan and Hydrochlorothiazide Tablets USP de 150 mg,/12.5 mg y 300 mg/12.5 mg.
Estas tabletas están empaquetadas en frascos de 30 y 90 unidades; fueron distribuídas en gran parte de Estados Unidos a mayoristas, farmacias con entregas por correo, supermercados y cadenas de farmacias físicas.
Si bien la marca no ha recibido ningún reporte de usuarios afectados, está haciendo efectivo los retiros como medida de precaución y notificando a los distribuidores y cadenas que recibieron los lotes para que los usuarios que lo compraron devuelvan el producto.
Asimismo, tanto la FDA como la marca, recomiendan a los pacientes con presión arterial que compraron la línea de tabletas que no las consuman y que consulten con su médico para que les prescriba un nuevo medicamento o uno similar al retirado.
La tableta de Irbesartan USP retirada es un bloqueador del receptor de angiotensina II, describe la FDA, indicado para el tratamiento de la hipertensión, la nefropatía diabética en pacientes hipertensos con diabetes de tipo II.
En tanto, el Ibersartan e Hidroclorotizada comprimidos USP se trata de irbesartán, un antagonista del receptor de angiotensina II, indicado para la hipertensión en pacientes que no se controlan con monoterapia o con terapias iniciales.
No te pierdas de las últimas noticias de Vive Usa en Google News, síguenos aquí
[Publicidad]